二、伦理批件及更新批件递交
药物临床试验机构 次 (0)次
递交伦理资料流程
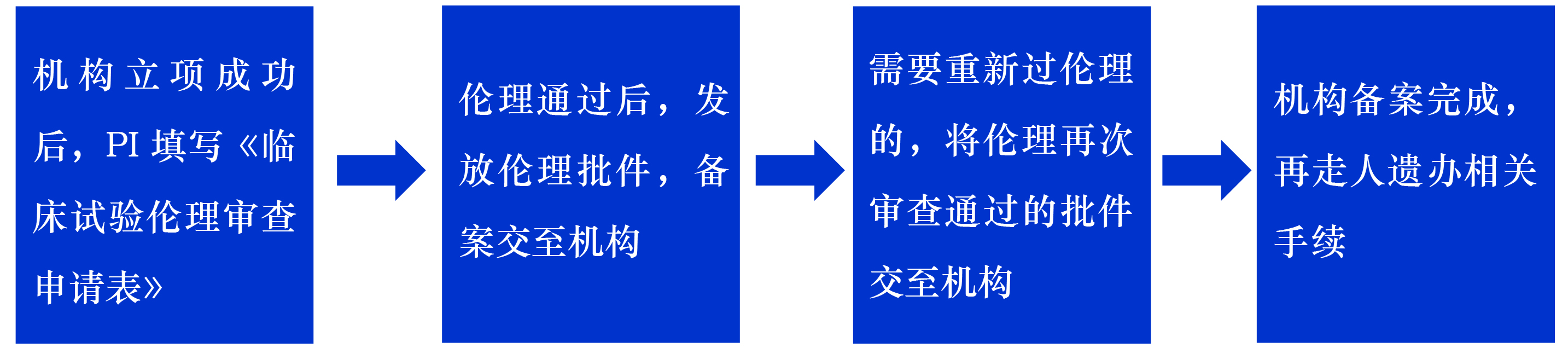
注意事项:
1. 过伦理须在机构立项完成之后,立项审核表经机构主任签字确认后。
2. 伦理批件须在更新后24小时内将复印件交至机构备案。
3. 向本院伦理委员会提供资料包括临床试验伦理审查申请表、研究者简历、研究小组成员名单。
临床试验伦理审查申请表(点击下载)
 |
药物临床试验伦理审查申请表 |
研究小组成员名单(点击下载)
 |
研究小组成员名单 |




